Пенициллин изобретение 20 века. Пенициллин: как открытие Флеминга превратилось в антибиотик
Сколько случайностей привело к открытию одного из самых действенных лекарств XX века и как этому помогли окно лаборатории и стена бомбоубежища, читайте в рубрике «История науки».
13 сентября 1929 года шотландский бактериолог Александр Флеминг на заседании Медицинского исследовательского клуба при больнице св. Марии Лондонского университета впервые сообщил о том, что открыл первый антибиотик - пенициллин. Впоследствии признавали, что пенициллин стал одним из самых великих медицинских открытий двадцатого века, а этот век и без того был весьма богат на открытия в медицине. Как бы там ни было, в 1945 году Флеминг стал одним из лауреатов Нобелевской премии, присужденной именно за открытие пенициллина.
В своей Нобелевской речи Флеминг тогда заявил: «Говорят, что я изобрел пенициллин. Но ни один человек не мог его изобрести, потому что это вещество создано природой. Я не изобретал пенициллин, я всего лишь обратил на него внимание людей и дал ему название». На самом деле ситуация с пенициллином еще интереснее: похоже, что природе пришлось изрядно потрудиться и устроить целую сеть случайностей, чтобы заставить людей, в первую очередь самого Флеминга, открыть это вещество.
Начать нужно с того, что Флеминг стал врачом отчасти благодаря случайности. Учитывая весь спектр его талантов, наш герой вполне мог выбрать и другое научное направление, даже заняться искусством (с детства он увлекался живописью) или стать военным. По совету старшего брата он выбрал медицину и подал документы на национальный конкурс для поступления в медицинскую школу при больнице св. Марии. Получив на экзамене высшие баллы и став хирургом по окончании обучения, Флеминг связал с этой больницей всю свою оставшуюся жизнь.
Александр Флеминг
Imperial War Museums/Wikimedia Commons
Он стал работать в лаборатории исследования ран и проявил свои таланты исследователя, показав, что карболовая кислота, в то время широко применявшаяся для обработки открытых ран, не подходит в качестве антисептика. Дело в том, что она убивает создающие в организме защитный барьер лейкоциты и в конечном счете способствует выживанию в тканях болезнетворных бактерий.
Следующая случайность произошла с Флемингом в 1922 году, когда он открыл фермент, впоследствии названный лизоцимом. Этот фермент убивал некоторые бактерии, не причиняя вреда здоровым тканям. Случайность здесь заключалась в том, что ученый был не слишком-то аккуратен и не очень любил приводить в порядок свой лабораторный стол. Однажды, будучи простужен, он чихнул в чашку Петри, где выращивал бактерии в питательной среде, и не продезинфицировал ее, как того требовали правила. Через несколько дней по цвету остатков в этой чашке он обнаружил, что в местах, куда попала его слюна, бактерии были уничтожены.

Плесневелый грибок, содержащий пенициллин
Wikimedia Commons
Правда, в качестве антисептика лизоцим работал не слишком удачно: на большинство бактерий он действовал очень медленно, поэтому Флеминг поначалу стал использовать лизоцим при написании авангардных картин, где разные цвета на полотне создавались различными бактериями. Чтобы эти бактерии не переползали с одного цветового пятна на другое, он обрабатывал лизоцимом границы таких пятен.
Впрочем, в лаборатории Флеминг больше думал о поисках хорошего антисептика, чем о своей живописи. И в 1928 году история с его неаккуратностью повторилась. Каким-то чудом в одну из его не продезинфицированных чашек Петри, где он высеивал колонию золотистого стафилококка, попала плесень из соседней лаборатории - довольно редкий плесневый грибок Penicillium notatum . Через пару дней она растворила высеянную культуру, и там, где она попала в чашку, вместо желтой мутной массы виднелись капли, похожие на росу.
Здесь Флеминга озарило: он предположил, что смертоносное влияние на бактерии оказал плесневый грибок. Это предположение подтвердилось, и ученый получил из этого грибка вещество интенсивного желтого цвета, которое он и назвал пенициллином.
Обнаружилось, что даже разведенный в 500-800 раз пенициллин подавлял рост не только стафилококков, но также и стрептококков, пневмококков, гонококков, дифтерийной палочки и бацилл сибирской язвы, но не действовал на кишечную палочку, тифозную палочку и возбудителей гриппа, паратифа, холеры. Чрезвычайно важным открытием было отсутствие вредного влияния пенициллина на лейкоциты человека даже в дозах, во много раз превышающих губительную для стафилококков дозу. Это означало, что пенициллин для людей безвреден.
На изучение свойств открытого им вещества Флеминг потратил около года, и, хотя в чистом виде так и не сумел его получить, он все же решил рассказать о нем коллегам.
Настоящим антибиотиком пенициллин Флеминга стал значительно позже, после того как его исследования в 1938 году продолжили профессор Оксфордского университета, патолог и биохимик Говард Флори и химик Эрнст Борис Чейн, эмигрировавший из Германии после прихода к власти нацистов. Спустя год попыток ученым удалось сделать то, что не удалось Флемингу, - получить первые 100 миллиграмм чистого пенициллина. Однако грибок, из которого пенициллин был получен, оказался слишком капризным, требовалось найти ему более «послушную» и эффективную замену.

Говард Флори и Эрнст Борис Чейн
Wikimedia Commons
Для этой цели Чейн привлек к работе других специалистов: бактериологов, химиков и врачей. Была сформирована так называемая Оксфордская группа. Работа группы оказалась удачной, и в 1941 году пенициллин впервые спас от верной смерти человека с заражением крови - им стал 15-летний подросток.
Разгоревшаяся к тому времени война не позволила наладить в Англии массовое производство пенициллина, и летом 1941 года Оксфордская группа отправилась совершенствовать технологию в США. На экстракте американской кукурузы выход пенициллина увеличился в 20 раз. Затем решили поискать новые штаммы плесени, более продуктивные, чем Penicillium notatum , когда-то прилетевший в окно Флемингу. В лабораторию группы стали поступать образцы плесеней со всего мира. Группа также пополнилась Мэри Хант, которую вскоре прозвали «Заплесневелой Мэри», ведь она закупала на рынке все заплесневелые продукты. Случилось так, что именно она принесла с рынка гнилую дыню, в которой и был найден тот высокопродуктивный штамм, который ученые и искали, - P. Chrysogenum .
На основе этого штамма была разработана технология массового производства пенициллина. В 1945 году выпуск этого лекарства достиг 15 тонн в год, а в 1950-м - 150 тонн.
Механизм действия пенициллинов оказался весьма сложным, и только в 1957 году его прояснил американский исследователь Джеймс Парк, который открыл нуклеотид, подавляющий рост клеточной стенки многих микробов.

Модель химической структуры пенициллина
Wikimedia Commons
Дальнейшие исследования показали и главный недостаток пенициллинов: болезнетворные микроорганизмы быстро привыкали к их присутствию. Так, если в 1945 году гонорея полностью излечивалась одной-единственной инъекцией пенициллина в 300 тысяч единиц, то в начале семидесятых для этого нужен был курс в десять раз более мощных инъекций. По состоянию же на 1998 год 78% гонококков развили устойчивость к антибиотикам группы пенициллина. По этой причине любой антибиотик был и остается главным лекарством XX века. В XXI веке ученые стоят перед проблемой создания нового лекарства, к которому микробы привыкнуть уже не смогут.
Любопытна судьба рождения пенициллина в СССР. В 1941 году разведка получила сведения о том, что в Англии создается чудодейственный антимикробный препарат на основе какого-то вида плесневых грибков. Тут же у нас начались работы в этом направлении, и уже в 1942 году микробиолог Зинаида Ермольева получила пенициллин из плесени Penicillium crustosum , взятой со стены одного из бомбоубежищ Москвы. В 1944 году препарат был с успехом опробован на раненых солдатах.

Зинаида Ермольева
Wikimedia Commons
Однако советский пенициллин, при всей значительности этого результата, был несовершенен и не мог производиться в необходимых для фронта количествах. К тому же у пациентов из-за него сильно повышалась температура, тогда как западный пенициллин никаких побочных последствий не вызывал. Купить в США технологии массового производства этого «лекарства века» не представлялось возможным, поскольку за океаном существовал запрет на продажу любых технологий, связанных с пенициллином.
Ситуацию тогда спас Эрнст Чейн, который был автором английского патента на получение пенициллина. Он предложил свою помощь Советскому Союзу, и в 1948 году с его помощью наши ученые сумели разработать необходимую технологию, по которой один из московских фармацевтических заводов тут же стал производить лекарство.
В 1945 году Александр Флеминг, Говард Флори и Эрнст Борис Чейн были удостоены Нобелевской премии по физиологии и медицине. В Нобелевской лекции Флеминг отметил, что «феноменальный успех пенициллина привел к интенсивному изучению антибактериальных свойств плесеней и других низших представителей растительного мира. Лишь немногие из них обладают такими свойствами».
В оставшиеся десять лет жизни ученый был удостоен 25 почетных степеней, 26 медалей, 18 премий, 30 наград и почетного членства в 89 академиях наук и научных обществах.
11 марта 1955 года Флеминг умер от инфаркта миокарда. Его похоронили в соборе Св. Павла в Лондоне - рядом с самыми почитаемыми британцами. В Греции, где бывал ученый, в день его смерти объявили национальный траур. А в испанской Барселоне все цветочницы города высыпали охапки цветов из своих корзин к мемориальной доске с именем великого бактериолога и врача.
ЧАСТЬ I
Глава 1
ИЗОБРЕТЕНИЕ ПЕНИЦИЛЛИНА
Судьба одаривает только подготовленные умы.
Луи Пастер

НЕВИДИМЫЕ ВРАГИ
На протяжении многих веков и далее тысячелетий миллионы людей гибли от врагов, невидимых невооруженным глазом. Эти враги – микробы. История человечества – это история больших и малых войн, однако можно с уверенностью утверждать, что жертвами микроскопических бактерий пали куда больше людей, чем во всех войнах, вместе взятых. Достаточно вспомнить ужасающие эпидемии оспы, чумы или хотя бы гриппа, которые в Средние века буквально выкашивали до половины населения Европы и даже более. К этому списку надо добавить раневую инфекцию и фатальные осложнения безобидных по нынешним меркам мелких бытовых травм. Известно, что в XVI в. средняя продолжительность жизни человека составляла около 30 лет. Что такое для современного человека порезаться ножом для резки хлеба на кухне или наступить на гвоздь? Неприятность, не более того. А еще в начале ХХ в. (по историческим меркам – совсем недавно) такая мелочь легко могла бы унести пострадавшего в могилу.
ПЕРВЫЙ ШАГ К ПОБЕДЕ
Положение дел существенно изменилось благодаря английскому хирургу Д. Листеру, который установил, что инфекционные осложнения, приводящие к огромной послеоперационной смертности, вызываются микроорганизмами, внесенными в рану извне. Он в 1867 г. разработал и теоретически обосновал метод борьбы с ними, названный антисептикой. Сущность метода заключается в уничтожении попавших в рану микробов. Однако в корне изменило ситуацию открытие английского (точнее, шотландского) микробиолога А. Флеминга (1881–1955), которое, как и многие другие великие открытия, не обошлось без нелепых, но счастливых случайностей, что, впрочем, ни в коей мере не умаляет заслуг ученого. Ему удалось из обычной, казалось бы, плесени выделить первый антибиотик – пенициллин. Самыми значимыми достижениями в терапии заболеваний инфекционной природы на рубеже веков стали первые вакцины, а также учение о фагоцитах И. И. Мечникова. Все они базировались на мобилизации естественных сил человеческого организма для борьбы с болезнью. Ведущие врачи и бактериологи того времени небезосновательно предполагали, что дальнейший прогресс в медицине будет связан с попытками усилить или каким-то образом дополнить свойства иммунной системы человека.
СПАСИТЕЛЬ ЧЕЛОВЕЧЕСТВА
Александер Флеминг родился в Великобритании в графстве Эйршир в семье фермера Хью Флеминга от его второй жены Грейс. Когда мальчику исполнилось 7 лет, умер его отец, и матери пришлось самой управляться с фермой. А. Флеминг посещал небольшую сельскую школу, находившуюся неподалеку от их фермы, а позже Килмарнокскую академию. Он рано проявил интерес к естествознанию. В возрасте 13 лет он уехал в Лондон, где поступил на работу клерком. Параллельно юный А. Флеминг посещал занятия в Политехническом институте на Риджент-стрит, а в 1900 г. вступил в Лондонский шотландский полк. А. Флеминг заслужил репутацию отличного стрелка и спортсмена; к тому времени уже закончилась Англо-бурская война, и ему не довелось служить за пределами Великобритании. Спустя год он получил от дяди наследство в 250 фунтов стерлингов – изрядную по тем временам сумму – и, последовав совету старшего брата, работавшего в Лондоне врачом, принял участие в национальном конкурсе для поступления в медицинскую школу. На экзаменах он отличился, получив самые высокие баллы, и стал стипендиатом медицинской школы, которая существовала при больнице Св. Марии. А. Флеминг изучал хирургию и, успешно сдав экзамены, в 1906 г. стал членом Королевского хирургического колледжа. Одним из наиболее выдающихся ученых в больнице Св. Марии был профессор Алмрот Райт, известный бактериолог и иммунолог. С 1906 г. А. Флеминг работал в бактериологической лаборатории под его руководством; в 1908 г. он получил степени бакалавра и магистра наук в Лондонском университете. Во время Первой мировой войны служил в чине капитана армейским врачом во Франции под началом А. Райта. На войне как на войне – вопрос об иммунизации даже не поднимался, были проблемы куда более насущные: раненые тысячами погибали от заражения крови, столбняка и гангрены. В тщетных попытках спасти их хирурги использовали антисептические средства. А. Флеминг, тщательно изучив инфицированные раны, доказал полную непригодность антисептиков для терапии в этих случаях. Более того, он выяснил, что карболовая кислота, применявшаяся в качестве основного антисептика при лечении открытых ран, уничтожает лейкоциты, тем самым разрушая защитный барьер организма и способствуя выживанию в ране бактерий. До главного открытия всей жизни А. Флеминга оставалось чуть более 10 лет.
НОВОЕ ИЗОБРЕТЕНИЕ ЗАСЛУГА МНОГИХ
Не следует считать пенициллин единственной заслугой А. Флеминга; еще в 1922 г. он совершил свое первое важное открытие – выделил из человеческих тканей вещество, обладающее способностью довольно активно растворять некоторые виды микробов. Открытие это было сделано почти случайно при попытке выделить бактерии – возбудители обычной простуды. Профессор А. Райт, под чьим руководством А. Флеминг продолжал свою исследовательскую работу, назвал новое вещество лизоцимом (лизис – разрушение микроорганизмов). Правда, оказалось, что лизоцим малоэффективен в борьбе с наиболее опасными болезнетворными микробами, хотя успешно уничтожает относительно менее опасные микроорганизмы. Таким образом, применение лизоцима в медицинской практике имело не очень широкие перспективы. Это подтолкнуло А. Флеминга к дальнейшему поиску эффективных и при этом по возможности безвредных для человека антибактериальных препаратов. Надо сказать, что еще в 1908 г. он проводил эксперименты с препаратом под названием «сальварсан», который лаборатория профессора А. Райта получила для всесторонних исследований в числе первых в Европе. Препарат этот был создан талантливым немецким ученым П. Эрлихом (Нобелевская премия совместно с И. И. Мечниковым, 1908 г.). Тот искал препарат, убийственный для болезнетворных микроорганизмов, но безопасный для пациента, так называемую магическую пулю. Сальварсан был довольно эффективным противосифилитическим средством, но оказывал на организм побочное действие токсического характера. Это были лишь первые маленькие шаги в сторону создания современных противомикробных и химиотерапевтических препаратов. Известно, что еще в XV–XVI вв. в народной медицине для лечения гноящихся ран использовалась зеленая плесень. Ею, например, умела лечить Алена Арзамасская, сподвижница Степана Разина, русская Жанна д’Арк. Попытки накладывать плесень непосредственно на раневую поверхность давали, как это ни странно, хорошие результаты. Базируясь на учении об антибиозе (подавлении одних микроорганизмов другими), основы которого были заложены Л. Пастером и нашим великим соотечественником И. И. Мечниковым, А. Флеминг в 1929 г. установил, что лечебное действие зеленой плесени обусловлено особым веществом, выделяемым ею в окружающую среду.
ВСЕ ГЕНИАЛЬНОЕ ОТКРЫВАЕТСЯ СЛУЧАЙНО?
Попытаемся воссоздать цепь почти невероятных случайностей и совпадений, предшествовавших великому открытию. Первопричиной стала, как ни странно, неряшливость А. Флеминга. Рассеянность свойственна многим ученым, но далеко не всегда она приводит к таким позитивным результатам. Итак, А. Флеминг не очищал чашки из-под исследуемых культур по нескольку недель, в итоге его рабочее место оказывалось заваленным полусотней чашек. Правда, в процессе уборки он скрупулезно исследовал каждую чашку из опасения пропустить что-либо важное. И не пропустил. В один прекрасный день он обнаружил в одной из чашек пушистую плесень, которая подавляла рост посеянной в этой чашке культуры стафилококков. Выглядело это так: цепочки стафилококков вокруг плесени исчезли, и на месте желтой мутной массы виднелись капли, напоминавшие росу. Убрав плесень, А. Флеминг увидел, что «бульон, на котором разрослась плесень, приобрел отчетливо выраженную способность подавлять рост микроорганизмов, а также бактерицидные и бактериологические свойства по отношению ко многим распространенным патогенным бактериям». По всей видимости, споры плесени были занесены через окно из лаборатории, где культивировались образцы плесени, взятые из домов пациентов, страдающих бронхиальной астмой, для получения десенсибилизирующих экстрактов. Ученый оставил чашку на столе и уехал на отдых. Лондонская погода сыграла свою роль: похолодание благоприятствовало росту плесени, а последовавшее потепление – росту бактерий. Если бы из цепочки случайных совпадений выпало хотя бы одно событие, кто знает, когда бы человечество узнало про пенициллин. Плесень, которой была заражена культура стафилококков, относилась к довольно редкому виду рода Penicillium – P. notatum, который был впервые найден на сгнившем иссопе (полукустарниковом растении, содержащем эфирное масло и использующемся в качестве пряности); интересно, что в Библии мы встречаем невероятно точное указание на свойства этого растения. Вот фрагмент Псалма 50, который, кстати, вспомнил и А. Флеминг: «Окропи меня иссопом, и буду чист; омой меня, и буду белее снега». Первое упоминание об антибактериальной терапии?
ДОСТОИНСТВА НОВОГО ИЗОБРЕТЕНИЯ
В ходе дальнейших исследований выяснилось, что, к счастью, даже в больших дозах пенициллин нетоксичен для подопытных животных и способен убивать весьма устойчивые болезнетворные микроорганизмы. В больнице Св. Марии не было биохимиков, в результате чего не удалось выделить пенициллин в пригодном для инъекций виде. Эту работу провели в Оксфорде Х. У. Флори и Э. Б. Чейн лишь в 1938 г. Пенициллин канул бы в небытие, если бы ранее не произошло открытие А. Флемингом лизоцима (вот тут-то он действительно пригодился!). Именно это открытие подвигло оксфордских ученых заняться изучением лечебных свойств пенициллина, в результате чего препарат был выделен в чистом виде в форме бензилпенициллина и испытан клинически. Уже самые первые исследования А. Флеминга дали целый ряд бесценных сведений о пенициллине. Он писал, что это «эффективная антибактериальная субстанция, оказывающая выраженное действие на пиогенные (т. е. вызывающие образование гноя) кокки и палочки дифтерийной группы. Пенициллин даже в огромных дозах не токсичен для животных. Можно предположить, что он окажется эффективным антисептиком при наружной обработке участков, пораженных чувствительными к пенициллину микробами, или при его введении внутрь».
ЛЕКАРСТВО ПОЛУЧЕНО, НО КАК ЕГО ПРИМЕНЯТЬ?
Аналогично Пастеровскому институту в Париже, отделение вакцинации в больнице Св. Марии, где работал А. Флеминг, существовало и получало финансирование на исследования благодаря продаже вакцин. Ученый обнаружил, что в процессе приготовления вакцин пенициллин защищает культуры от стафилококка. Это было небольшое, но серьезное достижение, и А. Флеминг широко пользовался им, еженедельно отдавая указание изготовить большие партии бульона на основе пеницилла. Он делился образцами культуры Penicillium с коллегами в других лабораториях, но, как ни странно, А. Флеминг не сделал столь очевидного шага, который 12 лет спустя был предпринят Х. У. Флори и состоял в том, чтобы установить, будут ли спасены подопытные мыши от смертельной инфекции, если лечить их инъекциями пенициллинового бульона. Забегая вперед, скажем, что этим мышам исключительно повезло. А. Флеминг лишь назначил бульон нескольким пациентам для наружного применения. Однако результаты были весьма и весьма противоречивыми. Раствор не только с трудом поддавался очистке в значительном объеме, но и оказывался нестабильным. Кроме того, А. Флеминг ни разу не упомянул о пенициллине ни в одной из 27 статей или лекций, опубликованных им в 1930–1940 гг., даже когда речь в них шла о веществах, вызывающих гибель бактерий. Впрочем, это не помешало ученому получить все причитающиеся ему почести и Нобелевскую премию по физиологии и медицине в 1945 г.
Понадобилось длительное время, прежде чем ученые сделали заключение о безопасности пенициллина как для человека, так и для животного.
КТО ЖЕ ВСЕ-ТАКИ ПЕРВЫМ ИЗОБРЕЛ ПЕНИЦИЛЛИН?
А что в это время происходило в лабораториях нашей страны? Неужели отечественные ученые сидели сложа руки? Конечно, это не так. Многие читали трилогию В. А. Каверина «Открытая книга», однако далеко не все знают, что у главной героини, доктора Татьяны Власенковой, был прототип – Зинаида Виссарионовна Ермольева (1898 -1974), выдающийся ученый-микробиолог, создатель целого ряда отечественных антибиотиков. Кроме того, 3. В. Ермольева первой из отечественных ученых начала изучать интерферон как противовирусное средство. Действительный член АМН, она внесла огромный вклад в российскую науку. На выбор профессии 3. В. Ермольевой повлияла история смерти ее любимого композитора. Известно, что П. И. Чайковский скончался, заразившись холерой. По окончании университета 3. В. Ермольева была оставлена ассистентом на кафедре микробиологии; одновременно она заведовала бактериологическим отделением Северо-Кавказского бактериологического института. Когда в 1922 г. в Ростове-на-Дону вспыхнула эпидемия холеры, она, игнорируя смертельную опасность, изучала это заболевание, что называется, на месте. Позже она провела опаснейший эксперимент с самозаражением, результатом которого стало значительное научное открытие. В годы Великой Отечественной войны, наблюдая за ранеными, З. В. Ермольева видела, что многие из них умирают не непосредственно от ран, а от заражения крови. К тому времени исследования ее лаборатории абсолютно независимо от англичан показали, что некоторые плесени задерживают рост бактерий. З. В. Ермольева, разумеется, знала, что в 1929 г. А. Флеминг получил из плесени пенициллин, но выделить его в чистом виде так и не смог, т. к. препарат оказался весьма нестойким. Знала она и о том, что уже давно наши соотечественники еще на уровне народной медицины, знахарства заметили лечебные свойства плесени. Но при этом в отличие от А. Флеминга З. В. Ермольеву судьба не баловала счастливыми случайностями. В 1943 г. У. Х. Флори и Э. Чейн смогли наладить выпуск пенициллина в промышленных масштабах, однако для этого им пришлось организовывать производство в США. З. В. Ермольева, на тот момент стоявшая во главе Всесоюзного института экспериментальной медицины, поставила перед собой цель получить пенициллин исключительно из отечественного сырья. Надо отдать должное ее упорству – в 1942 г. первые порции советского пенициллина были получены. Величайшей и неоспоримой заслугой З. В. Ермольевой явилось то, что она не только получила пенициллин, но и сумела наладить массовое производство первого отечественного антибиотика. При этом следует учесть, что шла Великая Отечественная война, остро ощущалась нехватка самых простых и нужных вещей. В то же время потребность в пенициллине росла. И З. В. Ермольева сделала невозможное: она сумела обеспечить не только количество, но и качество, вернее, силу препарата. Наш пенициллин был в 1, 4 раза действеннее англо-американского, что подтвердил сам профессор У. Х. Флори. Сколько раненых обязаны ей жизнью, не поддается даже примерному подсчету. Создание советского пенициллина стало своеобразным толчком для создания целого ряда других антибиотиков: первых отечественных образцов стрептомицина, тетрациклина, левомицетина и экмолина – первого антибиотика животного происхождения, выделенного из молок осетровых рыб. Относительно недавно появилось сообщение, за достоверность которого пока сложно ручаться. Вот оно: пенициллин был обнаружен еще до А. Флеминга неким студентом-медиком Эрнестом Августином Дюшенсне , который в своей диссертационной работе подробно описал открытый им удивительно эффективный препарат для борьбы с различными бактериями, пагубно влияющими на человеческий организм. Свое научное открытие Э. Дюшенсне закончить не получилось из-за скоротечной болезни, повлекшей за собой смерть. Однако А. Флеминг и понятия не имел об открытии молодого исследователя. И только совсем недавно в Леоне (Франция) была случайно найдена диссертация Э. Дюшенсне. Кстати, патент на изобретение пенициллина не выдан никому. А. Флеминг, Э. Чейн и У. Х. Флори, получившие за его открытие одну Нобелевскую премию на троих, наотрез отказались получать патенты. Они сочли, что вещество, обладающее всеми шансами спасти все человечество, не должно быть источником наживы, золотой жилой. Этот научный прорыв единственный таких масштабов, на который никто и никогда не предъявлял авторских прав. Стоит упомянуть, что, победив многие распространенные и опасные инфекционные болезни, пенициллин продлил человеческую жизнь в среднем на 30–35 лет!
НАЧАЛО ЭРЫ АНТИБИОТИКОВ
Итак, в медицине началась новая эра – эра антибиотиков . «Подобное лечится подобным» – этот принцип известен врачам с древнейших времен. Так почему бы не бороться с одними микроорганизмами при помощи других? Эффект превзошел самые смелые ожидания; кроме того, открытие пенициллина положило начало поиску новых антибиотиков и источников их получения. Пенициллинам на момент открытия были свойственны высокая химиотерапевтическая активность и широкий спектр действия, что приближало их к идеальным препаратам. Действие пенициллинов направлено на определенные «мишени» в клетках микроорганизмов, отсутствующие у животных клеток.
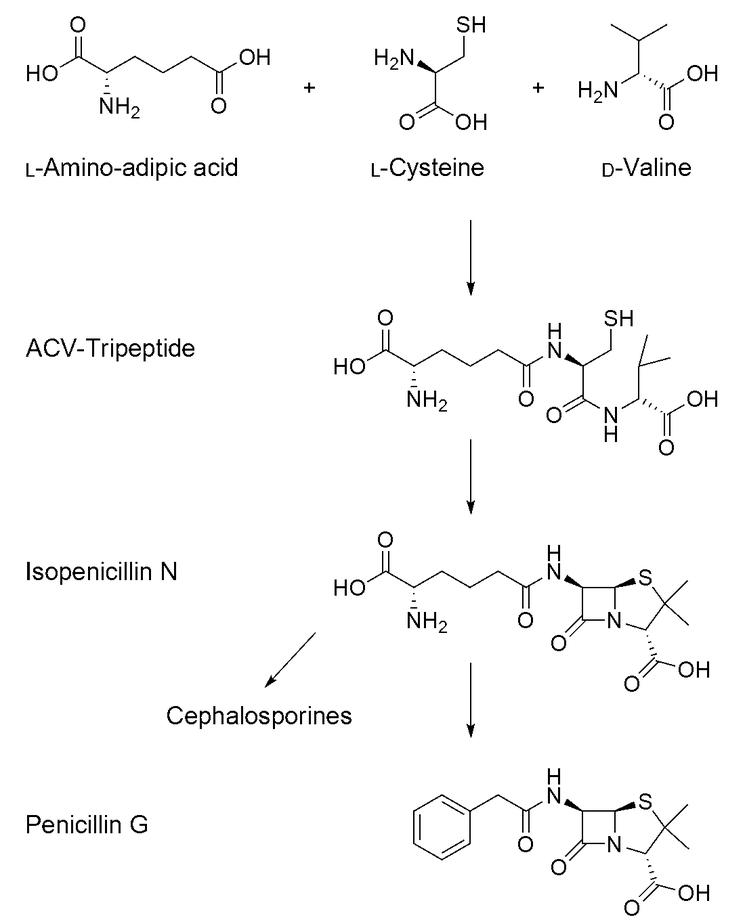
Справка. Пенициллины относятся к обширному классу гамма-лактамных антибиотиков. Сюда же относятся цефалоспорины, карбапенемы и монобактамы. Общим в структуре этих антибиотиков является наличие (3-лактамного кольца, (3-лактамные антибиотики составляют основу современной химиотерапии бактериальных инфекций.
АНТИБИОТИКИ НАПАДАЮТ БАКТЕРИИ ЗАЩИЩАЮТСЯ,
БАКТЕРИИ НАПАДАЮТ АНТИБИОТИКИ ЗАЩИЩАЮТСЯ

Пенициллины обладают бактерицидным свойством, т. е. губительно воздействуют на бактерии. Главный объект воздействия – это пенициллино-связывающие белки бактерий, которые являются ферментами заключительного этапа синтеза клеточной стенки бактерий. Блокирование антибиотиком синтеза пептидогликана приводит к нарушению синтеза клеточной стенки и в конечном счете к гибели бактерии. В процессе эволюции микробы научились защищаться. Они выделяют специальное вещество, разрушающее антибиотик. Это тоже фермент, носящий устрашающее название (3-лактамазы, которая разрушает (3-лактамное кольцо антибиотика. Но наука не стоит на месте, появились новые антибиотики, содержащие так называемые ингибиторы ((3-лактамаз – клавулановая кислота, клавуланат, сульбактам и тазобактам). Такие антибиотики называют пенициллиназозащищенными.
ОБЩИЕ ОСОБЕННОСТИ АНТИБАКТЕРИАЛЬНЫХ ПРЕПАРАТОВ
Антибиотики – это вещества, избирательно подавляющие жизнедеятельность микроорганизмов. Под «избирательным влиянием» подразумевается активность исключительно во взаимоотношении микроорганизмов при сохранении жизнеспособности клеток хозяина и воздействие не на все, а лишь на определенные роды и виды микроорганизмов. Например, фузидиевая кислота имеет высокую активность в отношении стафилококков, включая метициллинорезистентные, но не действует на пневмококки БГСА. С избирательностью близко связано представление об обширности спектра активности антибактериальных препаратов. Тем не менее с позиций сегодняшнего дня разделение антибиотиков на препараты широкого и узкого спектра действия представляется условным и подвергается серьезной критике по большей части из-за отсутствия критериев для такого деления. Неправильным является суждение о том, что лекарственные средства широкого круга действия являются более надежными, эффективными, более сильными, а использование антибиотиков с узким спектром в меньшей степени содействует развитию резистентности и т. д. При этом не учитывается приобретенная резистентность, вследствие чего, например, тетрациклины, которые в первые годы употребления были активными в отношении большинства клинически существенных микроорганизмов, в настоящее время лишились значительной части своего спектра активности, собственно, из-за формирования приобретенной резистентности у пневмококков, стафилококков, гонококков, энтеробактерий. Цефалоспорины III поколения, как правило, рассматривают как препараты с широким спектром активности при всем том, что они не действуют на MRSA, многие анаэробы, энтерококки, листерии, атипичные возбудители и др. Наиболее рационально рассматривать антибиотики с точки зрения клинической результативности при инфекции определенной органной локализации, так как клинические подтверждения эффективности, приобретенные в прекрасно наблюдаемых (сопоставительных, рандомизированных, проспективных) клинических экспериментах носят, бесспорно, более существенный характер, чем условный ярлык типа «антибиотик широкого (или узкого) спектра активности». Традиционно антибактериальные препараты делятся на природные (собственно антибиотики, например пенициллин), полусинтетические (продукты модификации природных молекул, например амоксициллин или цефазолин) и синтетические (например, сульфаниламиды, нитрофураны). В настоящее время такое деление потеряло актуальность, так как ряд природных антибиотиков получают путем синтеза (хлорамфеникол), а некоторые препараты (фторхинолоны), называющиеся «антибиотиками», являются синтетическими соединениями. Надлежит отличать антибиотики от антисептиков, которые воздействуют на микроорганизмы неизбирательно и используются для их уничтожения в живых тканях, и дезинфектантов, предназначенных для неизбирательного уничтожения микроорганизмов вне живого организма (для обеззараживания предметов ухода, поверхностей и пр.). Антибиотики представляют собой самую многочисленную группу лекарственных средств. Например, в России в настоящее время применяется 30 различных групп антибиотиков, а число препаратов приближается к 200. Все антибиотики, несмотря на различия химического строения и механизмов действия, связывает ряд уникальных особенностей. Во-первых, уникальность антибиотиков состоит в том, что, в отличие от большинства иных лекарственных средств, в их мишень-рецептор находится не в тканях человеческого организма, а в клетке микроорганизма. Во-вторых, динамичность антибиотиков не является долговременной, а снижается со временем, что обусловлено вырабатыванием лекарственной устойчивости (резистентности). Антибиотикорезистентность является непременным биологическим явлением, и предупредить ее практически невозможно. В-третьих, антибиотикорезистентные микроорганизмы представляют угрозу не только для пациента, у которого они были выделены, но и для многих остальных людей, даже разделенных временем и пространством. Вследствие этого борьба с антибиотикорезистентностью на сегодняшний день приобрела глобальные масштабы. Хорошо известно деление антибиотиков, как и прочих лекарственных препаратов, на группы и классы. Подобное разделение обладает большим значением с точки зрения понимания спектра активности, фармакокинетических признаков, характера нежелательных лекарственных реакций и т. д. Тем не менее ошибочно рассматривать все препараты, входящие в одну группу (класс, поколение), как взаимозаменяемые. Между препаратами одного поколения, различающимися только на одну молекулу, могут быть значительные различия. Например, среди цефалоспоринов III поколения клинически важной активностью в отношении синегнойной палочки обладают только цефтазидим и цефоперазон. Вследствие этого даже при приобретении данных о чувствительности синегнойной палочки к цефотаксиму или цефтриаксону эти препараты не следует использовать для лечения данной инфекции, так как результаты клинических испытаний подтверждают высокую частоту неэффективности. Вторым примером является отличие в фармакокинетике антибактериальных препаратов: цефалоспорины I поколения (цефазолин) не разрешается употреблять при лечении бактериального менингита вследствие плохой проницаемости через ГЭБ. Выделение бактерицидных и бактериостатических антибиотиков имеет основное практическое значение при лечении тяжелых инфекций, особенно у пациентов с нарушениями иммунитета, когда обязательно надлежит назначать бактерицидные препараты. Из фармакокинетических характеристик наиболее существенными при выборе препарата являются периоды частичного выведения и биологической доступности (что характерно для лекарств внутреннего применения). Следовательно, несмотря на многие совокупные черты, объединяющие антибактериальные препараты, при их назначении надлежит учитывать свойства каждого лекарственного средства и последствия их клинического использования, выявленные в хорошо проверяемых клинических испытаниях.
Открытие пенициллина продлило жизнь человека в среднем на 30 -35 лет. Ученые в своих исследованиях показали, как антибиотики борются с болезнетворными бактериями.
Безусловно, существует просто огромное количество лекарственных препаратов, всевозможных антибиотиков, БАДов, история открытия которых не известна людям и на сегодняшний день. Но вот что нельзя оставить без внимания, так это открытие такого известного антибиотика, как пенициллин.
Первым антибиотиком, который был открыт случайно, является именно легендарный пенициллин. Бензилпенициллин (пенициллин G (PCN G) или просто пенициллин (PCN)) - N-фенилацетамид 6-аминопенициллановой кислоты. Антибиотик, получаемый из плесневого гриба пенициллиума. Необходимо отметить тот момент, что его действие основывается на процессе подавления того синтеза, который участвует в оболочках внешнего типа, а также он относится еще и к клеткам бактериальной категории - бензилпенициллин препятствуют размножению клеток прокариот, в том числе и цианобактерий, а также препятствуют делению хлоропластов.
Примерно в 1929 году хорошо известный в то время британский бактериолог Александр Флеминг проводил серию экспериментов по изучению плесневых грибов. Он установил, что определенный вид плесневых грибов выделяет специфическое антибактериальное вещество, позже названное пенициллином. Именно его опыты были посвящены подробному изучению влияния бактериальных инфекций на организм человека.
После того как в ходе экспериментов были выращены первые колонии стафилококковых культур, Флеминг выявил, что большинство из них подвержены заражению плесневым грибом Penicillium chrysogenum. Британский ученый обратил свое внимание на ту область, где стафилококковые бактерии не размножались - как раз там, где находились плесневые грибы Penicillium notanum. Таким образом, он пришел к выводу, что определенного вида плесень способна вырабатывать вещества, которые просто убивают бактерии, соприкасающиеся с ней. Результатом экспериментов стало выделение бактериологом Флемингом антимикробного препарата, названного пенициллином. Словом, это бы первейший антибиотик современного типа.

Как действует пенициллин?
Что касается принципа работы прославленного антибиотика, то он заключается в том, что происходит процесс торможения и подавления химических реакций, необходимых для того, чтобы бактерии «жили». За счет действия пенициллина осуществляется блокирование молекул, которые участвуют в зарождении и строительстве совершенно новых клеток микробов. Мало того, очень важным необходимо считать и тот момент, что пенициллин G не оказывает практически никакого негативного влияния на организм человека, либо животного. Наружные оболочки клеток человека очень сильно отличаются от аналогичных клеток, которыми обладает бактерия.

Еще в 1931 году были предприняты попытки как-то улучшить само качество лекарственного препарата, а также получить его в весьма чистой форме. Но, к сожалению, на первых порах все это не увенчалось успехом, и до серийного производства пенициллина прошло еще около десяти лет.

В начале 40х годов 20го века английским бактериологам Хоуарду У. Флори, а также биохимикам Эрнсту Чейну и Норману У. Хитли впервые удалось получить качественную чистую форму пенициллина PCN G. Что спасло жизни сотен тысяч, если не миллионов раненных солдат во время второй мировой войны! Именно за это ученым была присуждена Нобелевская премия по физиологии и медицине «за открытие пенициллина и его целебного воздействия при различных инфекционных болезнях», Флеминг, Флори и Чейн получили её в 1945 году.

Именно благодаря пенициллину, было спасено огромное количество жизней, как во время второй мировой войны, так и после. Более того, лекарство стало первейшим средством, которое способно противостоять микробам самых различных классов и видов. Открытие и производство пенициллина является одним из величайших событий в медицине и науке ушедшего века.
Конечно, на сегодняшний день разработано немыслимое количество разнообразных антибиотиков, но всегда стоит помнить, что большинство из этих препаратов основаны именно на открытии лечебных свойств пенициллина!
За всю историю человечества не было другого лекарства, которое спасло бы столько жизней. В самом начале войны многие солдаты умирали не от ран, а от заражения крови. Пенициллин исцелил тысячи бойцов, которых считали безнадежными. История его открытия похожа на детектив, развязка которого подарила человечеству первый антибиотик, продливший продолжительность жизни примерно на 30 лет.
В 1928 году британский микробиолог Александр Флеминг обнаружил плесень, которая подавляла рост культуры стафилококков. Эта плесень относилась к редкому виду грибов рода Penicillium - P. Notatum.
Долгие годы специалисты пытались создать удобный для практического использования препарат на основе грибка, но безуспешно. Активное вещество лабораторной плесени не только с трудом поддавалось очистке, но и оказывалось нестабильным. Лишь в 1940 году в журнале The Lancet появилась первая статья об эффективном антибиотике - пенициллине. В условиях войны у Англии не было возможности разрабатывать технологию промышленного производства, и специалисты поняли: надо отправляться в США. Так в 1941 году фронт исследовательской работы переместился в Америку.
Западный фронт
Сама поездка оказалась нервной: было жарко, а плесневые грибы не выдерживают высокой температуры - их могли не довезти. В США перед учеными встала другая проблема: возможность промышленного производства пенициллина. Научные специалисты общались со многими учеными и фабрикантами, и в итоге в 1941 году обосновались в лаборатории города Пеории штата Иллинойс. Американские исследователи предложили новую питательную среду для выращивания плесневых грибов - кукурузный экстракт, которого в этом регионе США было много. Он оказался более чем пригодным для исследовательских целей.
Была еще одна задача - найти наиболее «продуктивный» штамм грибка. В лабораторию присылали образцы плесени со всего мира, но нужной среди них не было. Искали и на месте: наняли женщину, которая покупала заплесневелые продукты, - ее прозвали «плесневой Мэри».
В один прекрасный летний день 1943 года Мэри принесла в лабораторию полусгнившую дыню, а на ней - золотистую плесень Penicillium Chrysogenum, которая и оказалась именно той, что нужна была ученым. Из плесени получилось выделить самый эффективный штамм, и при этом его производство оказалось очень выгодным: стоимость лечения одного случая сепсиса снизилась с 200 до 6,5 доллара. Сегодняшний пенициллин - это потомок той самой плесени.
Наконец, председатель научно-исследовательского медицинского совета США Альфред Ричардс взял под крыло организацию производства - финансирование поступило через президента США Рузвельта. Первый завод построили меньше чем за год, и в течение первого года его работы производство пенициллина выросло в 100 раз.
В армии союзников антибиотики начали использовать в июле 1943 года во время высадки на Сицилии - случаи смерти от гангрены прекратились. По некоторым данным, с высадкой в Нормандии в июне 1944 года медлили не только по политическим соображениям, но и из-за опасений, что пенициллина не хватит.
Иногда бывает так, что великое открытие совершает тот, кто постоянно нарушает правила. Тысячи врачей, которые содержали свои рабочие места в чистоте, не смогли сделать того, что удалось неаккуратному Александру Флемингу — открыть первый в мире антибиотик. И вот что интересно: если бы он соблюдал чистоту, то у него бы тоже ничего не получилось.
Давным-давно великий французский химик Клод-Луи Бертолле весьма остроумно заметил: "Грязь — это вещество не на своем месте". Действительно, стоит только чему-то оказаться не там, где ему надлежит пребывать, и сразу же в помещении возникает беспорядок. А поскольку он весьма неудобен и для работы, и для нормальной жизни, то всех с детства учат, что следует чаще убираться. В противном случае количество вещества не на своем месте превысит таковое, свое место знающее.
Особенно нетерпимы к грязи медицинские работники. И их можно понять — вещество "не на своем месте" быстренько становится местом прописки разнообразных микроорганизмов. А они весьма опасны для здоровья как пациентов, так и самих врачей. Возможно, именно поэтому большинство медиков — патологические чистюли. Впрочем, не исключено, что в данный профессии существует своеобразный искусственный отбор — тот врач, что постоянно "кладет" вещество не на свое место, теряет клиентуру и уважение коллег и в профессии не задерживается.
Тем не менее, искусственный отбор, как и его естественный тезка, иногда дает сбой. Бывает, что доктор-грязнуля приносит человечеству куда больше пользы, чем его аккуратные коллеги. Именно о таком забавном парадоксе и пойдет речь — о том, как однажды неряшливость медика спасла жизни миллионов людей. Однако давайте обо всем по порядку.
6 августа 1881 года в шотландском городе Дарвел в семье фермеров Флемингов родился мальчик, которого назвали Александром. Ребенок с детства отличался любознательностью и тащил с улицы в дом все, что считал интересным. Его родителей это, правда, не раздражало, однако весьма огорчало то, что их отпрыск никогда не складывал свои трофеи в определенное место. Юный натуралист разбрасывал по дому и засушенных насекомых, и гербарии, и минералы и более опасные для здоровья вещи. Словом, как ни пытались приучить Александра к порядку и чистоте, все равно ничего из этого не вышло.

Через некоторое время Флеминг поступил в медицинскую школу при больнице святой Марии. Там Александр изучал хирургию и, выдержав экзамены, в 1906 году стал членом Королевского колледжа хирургов. Оставаясь работать в лаборатории патологии профессора Алмрота Райта больницы святой Марии, он в 1908 году получил степени магистра и бакалавра наук в Лондонском университете. Следует заметить, что медицинская практика не особенно интересовала Флеминга — куда больше его привлекала исследовательская деятельность.
Сослуживцы Александра неоднократно отмечали, что даже в лаборатории тот был ну просто чудовищно неаккуратен. А в его рабочий кабинет было опасно входить — реактивы, медикаменты и инструменты валялись вперемешку повсюду, а присаживаясь на стул, можно было напороться на скальпель или пинцет. Флеминг постоянно получал выговоры и порицания от старших коллег за то, что у него все лежит не на своем месте, однако, похоже, его это не особенно волновало.
Когда началась Первая Мировая война, молодой врач отравился на фронт во Францию. Там он, работая в полевых госпиталях, начал изучение инфекций, которые проникали в раны и вызывали тяжелые последствия. И вот уже в начале 1915 года Флеминг представил доклад, в котором рассказывалось о присутствии в ранах видов микробов, некоторые из которых были еще не знакомы большинству бактериологов. Ему также удалось выяснить, что применение антисептиков в течение нескольких часов после ранения не полностью уничтожает бактериальные инфекции, хотя многие хирурги так считали. Более того, самые зловредные микроорганизмы проникали в раны настолько глубоко, что уничтожить их простой антисептической обработкой было невозможно.

Что же следовало делать в подобных случаях? В возможности лечения таких инфекций при помощи традиционных лекарств из неорганических веществ Флеминг не особенно верил — его довоенные исследования терапии при сифилисе показали, что данные методы весьма ненадежны. Однако Александр был увлечен идеями своего шефа, профессора Райта, который считал использование антисептиков тупиковым путем, поскольку они ослабляют защитные свойства самого организма. А вот если получить препараты, которые будут стимулировать иммунитет, то пациент сможет сам уничтожить своих "обидчиков".
Развивая мысль своего коллеги, Флеминг предположил, что сам человеческий организм должен содержать вещества, убивающие микробов (следует заметить, что про антитела тогда толком ничего не знали, их удалось выделить только в 1939 году). Свою гипотезу ему удалось подтвердить экспериментально только после войны с использованием техники "слайд ячейки". Методика позволила легко показать, что при попадании микробов в кровь лейкоциты оказывают очень сильное бактерицидное действие, а при добавлении антисептиков эффект значительно снижается или даже полностью ликвидируется.
Итак, ободренный Флеминг стал экспериментировать с различными организменными жидкостями. Он поливал ими бактериальные культуры и анализировал результат. В 1922 году ученый, простудившись, шутки ради высморкался в чашку Петри, где росла бактериальная культура Micrococcus l ysodeicticus. Однако эта шутка привела к открытию — все микробы погибли, а Флемингу удалось выделить вещество лизоцим, обладающий антибактериальным действием.
Флеминг продолжил исследование данного естественного антисептика, однако вскоре выяснилось, что для большинства болезнетворных бактерий лизоцим безвреден. Однако ученый не сдавался и повторял эксперименты. Самое интересное, что Александр, работая с культурами самых опасных микроорганизмов, совершенно не изменял своим привычкам. По-прежнему его стол был завален чашками Петри, которые не мылись и не стерилизовались неделями. Коллеги боялись заходить в его кабинет, но неряшливого доктора, похоже, перспектива подхватить тяжелую болезнь нисколько не пугала.
И вот через семь лет удача вновь улыбнулась исследователю. В 1928 году Флеминг начал исследовал свойства стафилококков. Сначала работа не принесла ожидаемых результатов и доктор решил взять отпуск в конце лета. Тем не менее, он и не подумал убраться в своей лаборатории. Итак, Флеминг уехал отдыхать, так и не помыв чашек Петри, а когда 3 сентября вернулся, то заметил, что в одной чашке с культурами появились плесневые грибы, а присутствовавшие там колонии стафилококков погибли, в то время как другие колонии были в норме.
Заинтригованный Флеминг показал загрязненные грибами культуры своему бывшему помощнику Мерлину Цена, который сказал: "Вот так же вы и открыли лизоцим", что следует воспринимать не как восхищение, а как порицание за неаккуратность. Определив грибки, ученый понял, что антибактериальное вещество производит представитель вида Penicillium notatum , который попал на культуру стафилококков совершенно случайно. Спустя несколько месяцев, 7 марта 1929 года, Флеминг выделил таинственное антисептическое вещество и назвал его пенициллином. Так началась эра антибиотиков — лекарств, подавляющих бактериальные и грибковые инфекции.
И вот что интересно — до Флеминга многие ученые достаточно близко подошли к открытию подобных веществ. В СССР, например, всего в шаге от получения антибиотиков стоял Георгий Францевич Гаузе. Были прорывы на данном фронте у ученых из США и многих стран Европы. Однако никому это загадочное вещество в руки так и не далось. Наверное, это произошло потому, что все они были адептами чистоты и стерильности, и плесень Penicillium notatum просто не могла проникнуть в их лаборатории. А для того, чтобы раскрыть секрет пенициллина, потребовался именно грязнуля и неряха Александр Флеминг.